El dilema diario en la consulta
Imagina esta situación: llega a consulta un paciente de 35 años que ha terminado recientemente un tratamiento con antibióticos por una infección respiratoria. Comenta que ha experimentado molestias digestivas, alteraciones en sus deposiciones y sensación de hinchazón abdominal. En la farmacia le recomendaron "algo para la flora intestinal", pero no sabe si necesita prebióticos o probióticos.
Esta escena se repite constantemente en consultorios médicos, farmacias y centros de salud. La confusión entre prebióticos y probióticos no es solo del paciente común; también representa un desafío para muchos profesionales de la salud que buscan brindar recomendaciones precisas y basadas en evidencia.
¿Por qué es crucial dominar este tema?
La microbiota intestinal influye directamente en:
- Sistema inmunológico: 70% de nuestras defensas residen en el intestino
- Salud mental: el eje intestino-cerebro afecta estado de ánimo y cognición
- Metabolismo: regulación del peso y la glucemia
- Inflamación sistémica: prevención de enfermedades crónicas
Una recomendación inadecuada no solo puede ser ineficaz, sino que también puede generar gastos innecesarios para el paciente y pérdida de confianza en el tratamiento.
Definiciones Fundamentales: Aclarando Conceptos
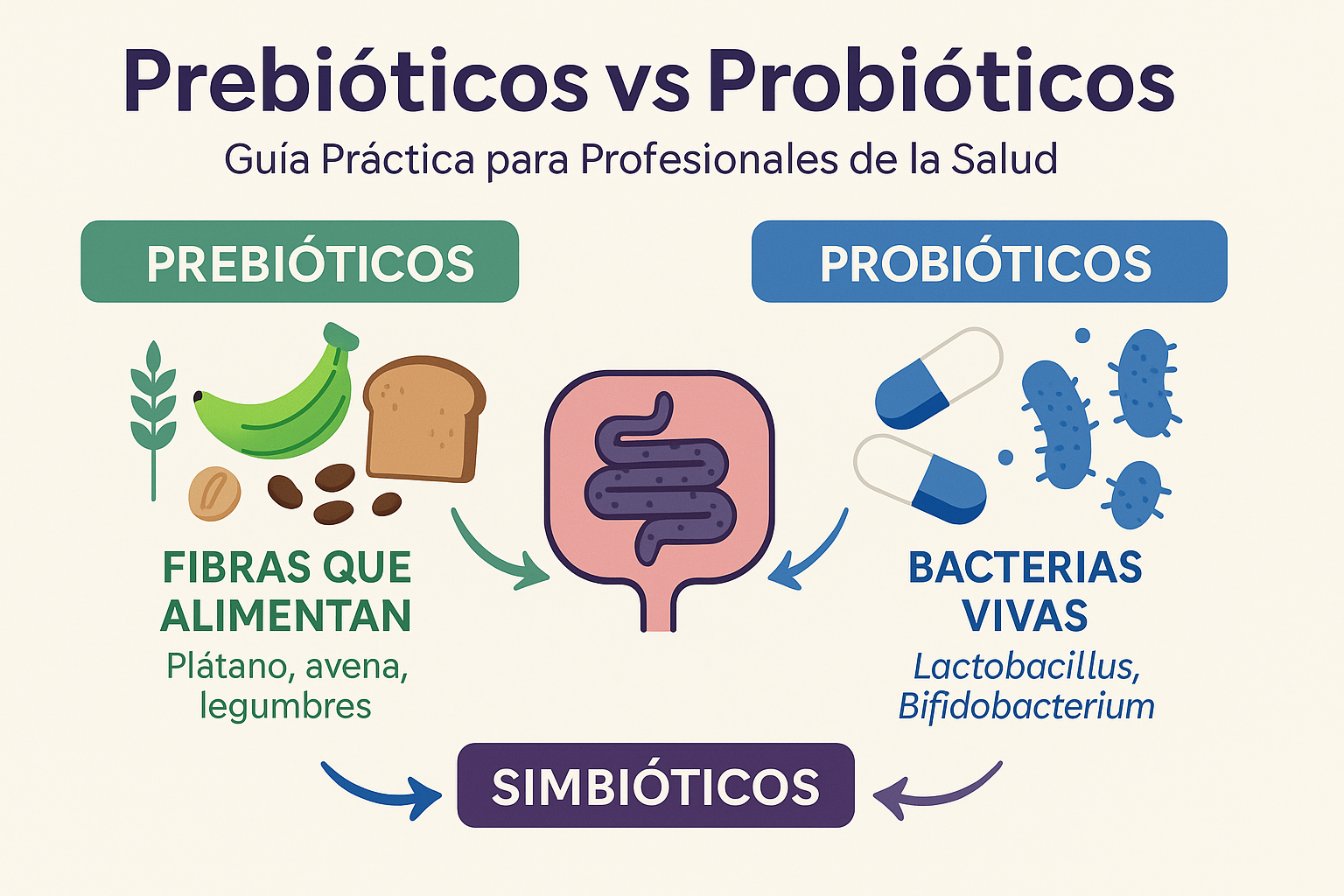
¿Qué son los Probióticos?
De acuerdo con la Organización Mundial de la Salud (OMS), los probióticos son microorganismos vivos que, cuando se administran en cantidades adecuadas, confieren un beneficio para la salud del huésped (Hill et al., 2014). Piénsalos como "soldados aliados" que llegan a reforzar el ejército intestinal.
Características clave:
- Microorganismos vivos (principalmente Lactobacillus y Bifidobacterium )
- Deben sobrevivir al tránsito gastrointestinal
- Se adhieren temporalmente a la mucosa intestinal
- Ejercen efectos beneficiosos mientras están presentes
Ejemplos comunes:
- Lactobacillus acidophilus
- Bifidobacterium longum
- Saccharomyces boulardii
- Lactobacillus rhamnosus GG
Mecanismos de Acción de los probióticos: ¿Cómo Funcionan?
Los probióticos ejercen sus efectos beneficiosos mediante múltiples mecanismos interconectados que actúan tanto a nivel local como sistémico. A nivel intestinal, estas bacterias benéficas fortalecen la barrera epitelial intestinal mediante el aumento de la producción de proteínas de unión estrecha (tight junctions) y estimulan la síntesis de mucina, creando una barrera física más robusta contra patógenos (Bermúdez-Brito et al., 2012).
Simultáneamente, los probióticos compiten directamente con microorganismos patógenos por sitios de adhesión en la mucosa intestinal y por nutrientes disponibles, fenómeno conocido como exclusión competitiva (Sánchez et al., 2019). A nivel bioquímico, producen sustancias antimicrobianas específicas como bacteriocinas, ácido láctico, peróxido de hidrógeno y diacetil, que modifican el ambiente intestinal creando condiciones desfavorables para el crecimiento de patógenos (Hawrelak & BNat, 2013). Desde la perspectiva inmunológica, los probióticos modulan tanto la respuesta inmune innata como la adaptativa, estimulando la producción de inmunoglobulina A secretora (IgA) y promoviendo la diferenciación de células T reguladoras, lo que resulta en una reducción de citoquinas proinflamatorias y un fortalecimiento de la tolerancia inmunológica (Cristofori et al., 2021).
¿Qué son los Prebióticos?
Los prebióticos son ingredientes fermentables selectivos que producen cambios específicos en la composición y/o actividad de la microbiota gastrointestinal, confiriendo beneficios para la salud (Gibson et al., 2017). Son el "alimento preferido" de las bacterias beneficiosas que ya tienes.
Características clave:
- Compuestos no digeribles por enzimas humanas
- Estimulan selectivamente el crecimiento de bacterias beneficiosas
- Fermentados principalmente en el colon
- Producen metabolitos beneficiosos (ácidos grasos de cadena corta)
Ejemplos comunes:
- Inulina
- Fructooligosacáridos (FOS)
- Galactooligosacáridos (GOS)
- Almidón resistente
Mecanismos de Acción de los prebióticos: ¿Cómo Funcionan?
Los prebióticos funcionan como "fertilizantes selectivos" que estimulan específicamente el crecimiento y la actividad metabólica de bacterias benéficas ya presentes en el microbioma intestinal. Su mecanismo de acción se basa en su resistencia a la digestión por enzimas humanas en el intestino delgado, llegando intactos al intestino donde son fermentados selectivamente por bacterias como Bifidobacterium y Lactobacillus (Gibson et al., 2017).
Durante este proceso de fermentación, se producen ácidos grasos de cadena corta (AGCC) —principalmente butirato, propionato y acetato— que actúan como metabolitos clave con múltiples funciones fisiológicas (Kumari et al., 2024). El butirato sirve como principal fuente de energía para los colonocitos, fortalece la integridad de la barrera intestinal y regula la expresión génica relacionada con la inflamación y el metabolismo celular (Li et al., 2023). Los AGCC también reducen el pH colónico, creando un ambiente desfavorable para patógenos mientras favorecen el crecimiento de bacterias beneficiosas. Adicionalmente, estos metabolitos ejercen efectos sistémicos al activar receptores acoplados a proteína G (GPR41, GPR43, GPR109A) presentes en diversos tejidos, modulando procesos como la homeostasis glucémica, la saciedad, la función inmune y la comunicación intestino-cerebro (Nicholson et al., 2021). A través de estos mecanismos, los prebióticos no solo nutren selectivamente la microbiota beneficiosa, sino que también generan un ambiente metabólico que promueve la salud intestinal y sistémica de manera sostenida.
Criterios de elección clínica: ¿cuándo usar cada uno?
Probióticos:
- Situaciones de depleción microbiana:
- Post-tratamiento antibiótico (hasta 2 meses después)
- Diarrea asociada a antibióticos (prevención y tratamiento) (McFarland, 2021)
- Gastroenteritis aguda
- Síndrome de intestino irritable con predominio de diarrea (Ford et al., 2020)
- Colitis ulcerosa en fase de remisión
O condiciones espacíficas como:
- Intolerancia a la lactosa (L. acidophilus)
- Prevención de infecciones urinarias recurrentes (L. rhamnosus GR-1)
- Dermatitis atópica en niños (L. rhamnosus GG)
Prebióticos:
Situaciones de mantenimiento a largo plazo:
- Estreñimiento crónico (Olveira et al., 2021)
- Síndrome de intestino irritable mixto (Ford et al., 2020)
- Prevención de cáncer colorrectal
- Mejora de la absorción de calcio
- Control de la glucemia en diabéticos tipo 2
También, puede aplicarse en poblaciones específicas:
- Adultos mayores (mejora de la diversidad microbiana)
- Personas con dieta baja en fibra
- Pacientes con síndrome metabólico
Terapia Combinada (Simbióticos):
Asocia el uso de probióticos y prebióticos, se presenta como una estrategia avanzada en el manejo de la salud intestinal. Su uso resulta especialmente indicado en procesos de reconstrucción post-antibiótica intensiva, en casos de enfermedad inflamatoria intestinal, en pacientes críticos con riesgo de traslocación bacteriana y como medida de apoyo en la preparación pre-quirúrgica gastrointestinal. De acuerdo con la evidencia científica (Swanson et al., 2020), esta intervención favorece la restauración del equilibrio microbiano, potencia la respuesta inmunitaria y contribuye a mejorar la evolución clínica en escenarios de alta vulnerabilidad.
Consideraciones Especiales por Población
Embarazo y Lactancia
- Probióticos: seguros, especialmente L. rhamnosus GG y B. animalis (Sanders et al., 2022)
- Prebióticos: reducir dosis por mayor sensibilidad gastrointestinal
Pediatría
- Probióticos: L. rhamnosus GG para diarrea, B. lactis para cólicos (Sanders et al., 2022)
- Prebióticos: GOS preferibles, dosis ajustadas por peso
Inmunodeprimidos
- Precaución con probióticos: riesgo de traslocación (consultar infectología)
- Prebióticos: generalmente seguros, benefician la barrera intestinal
Adultos Mayores
- Probióticos: B. longum mejora función inmune
- Prebióticos: inulina mejora diversidad microbiana y absorción de calcio (Nie et al., 2021)
Monitoreo y Seguimiento
Indicadores de Efectividad
|
Probióticos (2-4 semanas) |
Prebióticos (4-8 semanas) |
|
|
¿Cuándo Suspender o Cambiar?
- Probióticos: si no hay mejoría en 2 semanas o aparecen efectos adversos
- Prebióticos: si persisten molestias digestivas después de 2 semanas de adaptación
- Ambos: si aparecen síntomas nuevos o empeoramiento del cuadro clínico
Mensaje final: la personalización es clave
La elección entre prebióticos y probióticos no debe ser automática. Cada paciente es único, con su microbiota particular, historial médico específico y objetivos terapéuticos individuales.
La tendencia actual apunta hacia enfoques personalizados basados en análisis de microbiota, pero mientras esta tecnología se hace más accesible, una evaluación clínica cuidadosa y el seguimiento estrecho del paciente siguen siendo nuestras mejores herramientas.
Recuerda: los prebióticos alimentan lo que ya tienes, los probióticos agregan lo que necesitas. Esta simple frase puede ayudarte a tomar mejores decisiones clínicas y a explicar claramente las opciones a tus pacientes.
Referencias Científicas
- Hill, C., et al. (2014). Expert consensus document: The International Scientific Association for Probiotics and Prebiotics consensus statement on the scope and appropriate use of the term probiotic. Nature Reviews Gastroenterology & Hepatology, 11(8), 506-514.
- Gibson, G. R., et al. (2017). Expert consensus document: The International Scientific Association for Probiotics and Prebiotics (ISAPP) consensus statement on the definition and scope of prebiotics. Nature Reviews Gastroenterology & Hepatology, 14(8), 491-502.
- McFarland, L. V. (2021). Efficacy of prebiotics in the treatment of acute diarrhea in children: A systematic review and meta-analysis. Journal of Pediatric Gastroenterology and Nutrition, 73(4), 490-498.
- Swanson, K. S., et al. (2020). The International Scientific Association for Probiotics and Prebiotics (ISAPP) consensus statement on the definition and scope of synbiotics. Nature Reviews Gastroenterology & Hepatology, 17(11), 687-701.
- Sanders, M. E., et al. (2022). Probiotics and prebiotics for pediatric gastrointestinal disorders: A systematic review. Pediatrics, 149(3), e2021053990.
- Olveira, G., et al. (2021). Systematic review and meta-analysis: Effectiveness of prebiotics in irritable bowel syndrome. Clinical Nutrition, 40(7), 4298-4308.
- Nie, K., et al. (2021). Roseburia intestinalis: A beneficial gut organism from the discoveries in genus and species to its role in health and disease. Frontiers in Cellular and Infection Microbiology, 11, 757718.
- Ford, A. C., et al. (2020). Systematic review with meta-analysis: The efficacy of prebiotics, probiotics, synbiotics and antibiotics in irritable bowel syndrome. Alimentary Pharmacology & Therapeutics, 52(8), 1304-1319.
- Sánchez, B., Delgado, S., Blanco‐Míguez, A., Lourenço, A., Gueimonde, M., & Margolles, A. (2019). Adhesion mechanisms mediated by probiotics and prebiotics and their potential impact on human health. Applied Microbiology and Biotechnology, 103(16), 6463-6472.
